中商情报网讯:仿制药是指不需要太多的资金和尖端的技术,对国际或国内市场上已经出现的且在较大的范围内应用于临床治疗,临床应用的安全性和有效性相对明确,有比较成熟的合成方法、处方和制备工艺以及质量控制标准和质量控制方法的药品进行引进或模仿、研制生产出新药品的过程。
市场规模
中国仿制药市场在过去十年发展迅猛,仿制药规模近5000亿元,有近5000家药企,已有的药品批准文号总数高达18.9万个,仿制药在处方量中占比达95%。数据显示,2019年我国生物类似药市场规模突破1000亿美元,预计到2021年中国生物类似药市场将达1105亿美元。
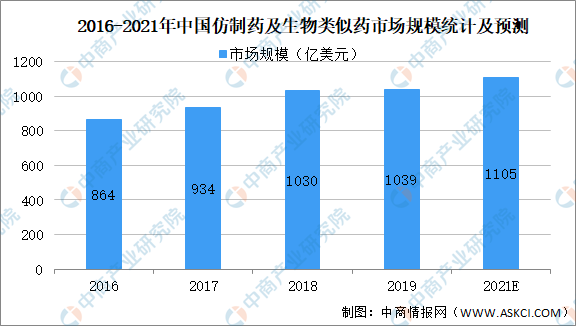
数据来源:弗若斯特沙利文、中商产业研究院整理
未来发展前景
1.一致性评价政策推动仿制药结构调整
2016年以来,仿制药一致性评价持续推进,深刻影响仿制药格局。通过一致性评价的仿制药将获得多方面的政策鼓励,包括在招标采购中可与原研药同组竞争,加速替代原研;无法通过一致性评价的品种可能逐步退出市场。一致性评价的推进,系我国药品质量安全水平保障与行业标准统一规范之有利举措,此举将促进产业集中度提高。2020年2月中共中央国务院发布《关于深化医疗保障制度改革的意见》,要求做好仿制药质量和疗效一致性评价受理与审评,通过完善医保支付标准和药品招标采购机制,支持优质仿制药研发和使用,促进仿制药替代。不断完善的行业政策有益于提高行业标准与药品质量安全水平,为优质制药企业的经营创造了健康、良好的环境与体制保障。
2.行业政策推动技术创新、鼓励优质仿制药替代
近年来,我国政府制定了一系列法规及政策以支持生物医药行业的发展。相关部委先后出台了《关于优化药品注册审评审批有关事宜的公告》、《关于改革完善仿制药供应保障及使用政策的意见》等文件,为医药行业内研发创新营造了良好的创新环境。其中国家药监局及国家卫生健康委员会于2018年共同发布《关于优化药品注册审评审批有关事宜的公告》,优先审评审批工作机制大幅缩短药品审评周期,进一步加速了药品的研发上市进程;药品上市许可人制度试点持续推进,并于2019年被正式纳入新版《中华人民共和国药品管理法》,标志着我国对于药品全生命周期管理的重视及愈发严格的要求;化学原料药、药用辅料及药包材与药品制剂关联审评审批制度逐步实施,相关事宜更加明确。
3.医疗改革的巨大推动作用
国家为建立具有中国特色的医疗卫生体制采取了各项有力措施,围绕分级诊疗、现代医院管理、全民医保、药品供应保障、综合监管五项基本医疗卫生制度和建立优质高效的医疗卫生服务体系,着力在解决“看病难”“看病贵”上持续发力,实施了一系列改革举措,取得重大阶段性成效。长期来看,医疗改革将对医药行业产生深远的影响,必将扩大整个市场的规模,并且推动更规范、更健康的竞争环境的形成。
更多资料请参考中商产业研究院发布的《中国仿制药行业市场前景及投资机会研究报告》,同时中商产业研究院还提供产业大数据、产业情报、产业研究报告、产业规划、园区规划、十四五规划、产业招商引资等服务。
 如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。
如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。

