中商情报网讯:合同研究组织(CRO)是通过合同形式为医药企业和医药科研机构在研发过程中提供专业外包服务的组织或机构。相比于欧美等发达国家的CRO市场,中国等新兴市场国家的CRO业务增长更加迅速。数据显示,2014年我国CRO市场规模仅18亿美元,到2018年我国CRO市场已达47亿美元,年均复合增长率约为28%。未来几年,中国CRO市场还将维持29.4%的年复合增长率,至2023年达到172亿美元,其中临床研究阶段CRO市场规模将达到133亿美元。
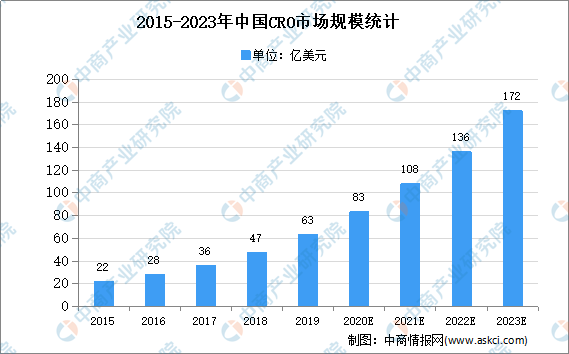
数据来源:Frost&Sulivan、中商产业研究院整理
CRO行业发展困境
1.高素质复合型人才的缺乏
CRO行业属于技术密集型行业,主要依靠专业人员提供技术服务。跨国CRO企业由于成立时间久,通过多年的培养和积累,储备了充足的高素质复合型人才以满足自身业务需要。CRO行业在国内起步较晚,行业内部的培训体系不够完善,从业人员水平参差不齐,专业人员需求缺口较大,同时因为资金和经营理念等问题,高素质复合型人才的缺乏一直是制约本土CRO企业发展的重要因素。
2.国内CRO行业集中度低
国外CRO行业经过40余年的发展,已产生多个业内巨头,占据行业主要市场。跨国CRO公司对我国本土临床试验熟悉程度不够,运营成本较高,但其有强大的资金实力、专业的技术人员和丰富的项目经验。我国CRO公司起步较晚,在面临跨国公司的竞争时整体上处于不利地位。此外,我国CRO行业集中度较低,大量的小型CRO公司只能完成临床试验外包服务中个别环节,未能形成规模化运营。近年来,我国对药物研发过程的质量管理监管要求日趋严格,逐渐向发达国家的监管要求靠拢。为保证临床试验数据的真实性和准确性,CFDA自2015年7月开展临床试验数据自查核查工作。随着我国CRO行业运营门槛提高,监管日趋严格,CRO企业需要加大软硬件投入以提高工作交付质量,增加了CRO公司的运营成本,依靠低价格竞争的小型CRO公司可能面临被淘汰的局面,大型CRO公司借此整合行业,预计未来行业集中度将逐渐提高。
CRO行业发展前景
1.产业政策的支持下,医药研发特别是创新药的研发投入快速增长
近年来,国家相继出台了一系列政策推动医疗健康产业的发展,支持医药研发投入。根据《国家中长期科学和技术发展规划纲要》,国务院组织实施了“重大新药创制”科技重大专项。《关于促进医药产业健康发展的指导意见》提出要促进创新能力提升,加强原研药、首仿药、中药、新型制剂、高端医疗器械等创新能力建设;推动重大药物产业化,继续推进新药创制。《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》提出要改革临床试验管理、加快上市审评审批、促进药品创新和仿制药发展。《医药工业发展规划指南》明确提出大力发展合同研发等新型生产性服务业,促进分工进一步专业化,提高效率和降低成本。
2.新药临床试验审批加速
自2015年起,CFDA启动了一系列改革以加快新药上市申请审批速度。根据NMPA发布的《2018年度药品审评报告》,2018年全年完成审评审批的注册申请共9,796件,2018年底排队等待审评审批的注册申请已由2015年9月高峰时的近22,000件降至3,440件(不含因申报资料缺陷等待申请人回复补充资料的注册申请),新药临床试验审批明显提速,审批速度的提升推升了制药企业在新药研发中的投入。
3.国内药企研发外包需求增加
随着我国人均寿命增加,老龄化趋势加剧以及慢性病发病率提升,人均医药消费需求预计将会快速增长,国内制药企业的研发投入亦会随之增长。制药企业为加速药品注册上市,委托CRO企业进行临床试验将缩短研发周期、降低研发成本。同时,在国家药品研发监管日益严格以及我国劳动力价格逐步升高的双重背景下,国内医药企业的研发成本也在不断升高,按照原有依靠企业自身建立完整研发链条的模式已无法适应当前激烈的竞争环境。因此,国内医药企业通过更多地委托CRO企业开展临床试验,以此缩短研发周期、降低资金成本。
4.跨国药企研发转移趋势明显
近年来,跨国企业由于专利药物到期、新药研发速度缓慢等原因,普遍面临收入增长放缓的压力。为了提高新药研发效率,跨国制药企业开始在全球范围整合研发体系,将部分研发工作转移到中国等新兴市场国家。中国具有庞大的人口基数,医药市场潜力巨大。且中国具有相关人才密集、疾病谱丰富、人力成本和原材料成本低廉等显著优势,成为跨国药企的重要研发基地之一。大量跨国企业在中国建立研发中心,将新药研发工作转移到中国开展,为我国CRO行业提供了更多发展机会。
更多资料请参考中商产业研究院发布的《中国CRO行业市场前景及投资机会研究报告》,同时中商产业研究院还提供产业大数据、产业情报、产业研究报告、产业规划、园区规划、十四五规划、产业招商引资等服务。
 如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。
如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。

