中商情报网讯:7月4日上午,《我不是药神》提档7月5日公映,比原定7月6日提前一天。据悉,目前点映累计票房已达1.08亿。《我不是药神》豆瓣开局9.0分,影片让人感受到生命在贫穷和疾病之间翻滚煎熬时的疼痛,同时引发网友对仿制药相关问题的热议。

印度专利政策宽松 仿制药出口额世界第一
《我不是药神》根据当年轰动一时的“药侠陆勇”的故事改编。影片讲述了神油店老板程勇帮助买不起进口抗癌药的慢粒白血病人,走私低价印度仿制药救命,并被病人尊为“药神”的故事。
所谓的仿制药,简单来理解就是仿已有国家标准的药品。在2005年之前,印度政府允许仿制专利药品。2005年,印度加入WTO,作为WTO协议的一部分,印度恢复了药品专利。不过,2005年1月生效的印度专利法只对1995年以后发明的新药、或经改进后能大幅度提高疗效的药物提供专利保护,而不支持原有药物混合或者衍生药物专利。
印度是全球第三大的药品生产国。在这宽松的专利条款的庇护下,印度仿制药迎来蓬勃发展。据IBEF数据统计显示,截至2015年,印度有10500个制药单元(工厂),3000多家药企。从规模上看,印度药品市场规模约占全球市场2.4%,生产的药品数量占比为10%。2016年印度药品市场规模为275.7亿美元,2011-2016年印度药品市场规模年均增速为5.64%,受多方面的利好等因素影响,预计2015-2020年市场将保持12.89%的年均增速,2020年印度药品市场规模或达到550亿美元。
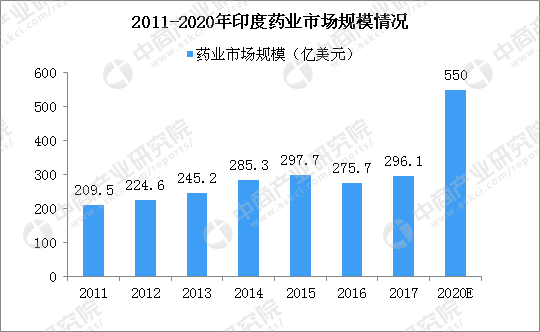
数据来源:IBEF 中商产业研究院整理
现在,印度作为全球最大的仿制药出口国,每年向全球100多个地区销售低价的仿制药,极大增强了全球患者的药物可及性。由于仿制药价格低廉,一些发达国家的患者也选择到印度就医或治疗,印度由此被称为“世界药房”。
多重利好 中国仿制药迎来发展机遇
近年来,中国面临医保支付压力不断增加的问题,对于质优价廉的仿制药需求增长明显,重磅创新药专利悬崖期的到来也为大量仿制药的上市提供了契机。
此外,全球仿制药的大型厂商主要集中于美国及欧洲地区,但是为了控制生产成本,仿制药巨头纷纷将生产基地向中国和印度等地转移,为中国仿制药发展提供了较好的发展机。
2015年以后医药行业再次整顿,国家各部门密集出台促进创新药研发和仿制药提升的政策。2016年2月国务院办公厅发布的《关于开展仿制药质量和疗效一致性评价的意见》指出,《基本药物目录》(2012年版)中,2007年10月1日前批准上市的化学药品仿制药、口服固体制剂共289个品种,应在2018年底前完成一致性评价。近两年的全国两会期间,多家药企两会代表呼吁,通过一致性评价的企业需要在招标、医保支付、医院准入等方面提供相应的政策。一致性评价推动仿制药提升质量。未来,若政府完善高质量仿制药招采的配套政策,才能真正把仿制药产业带入良性发展轨道。
2018年4月3日,国务院办公厅发布《关于改革完善仿制药供应保障及使用政策的意见》,从促进研发等三个方面提出十五条改革措施,推动仿制药发展。国家政策扶持,仿制药市场将进一步扩大。
前景光明 2020年仿制药市场规模逼近1.5万亿
中国是仿制药大国,中国医药工业信息中心数据显示,2016年我国仿制药市场规模约为9167亿元;受慢性病患病率逐年增加、人口老龄化、医保控费等因素影响,预计到2020年,我国仿制药市场规模可望达到14116亿元。
质量差价格高 中国仿制药如何破局?
其实,中国是仿制药大国,但不是强国。即使是仿制,也很难达到“高仿”。我国药品研发投入占药企销售额的比例大概是1%左右,国外一般是10%。我国药品在研发方面缺乏引导,产能分布不均衡。目前,中国仿制药长期面临着“安全、无效”的尴尬问题,质量远不及原研药。中国仿制药生产标准不一,导致我国仿制药在疗效方面差距巨大。
此外,由于国内仿制水平有限,仿制药质量较差,生产同质化严重,不少外资药企药物在专利期后,药价不但没有“断崖式”降价,反而高居不下。
针对中国仿制药行业问题,还需对阵下药。
1、抓好仿制药一致性评价
过去我国批准上市的药品没有与原研药一致性评价的强制性要求,所以有些药品在疗效上与原研药存在一些差距;此外,我国现代制药企业起步较晚,标准偏低,低标准的仿制药不仅制约了我国医药产业的创新发展,充斥其中的一些“安全基本无效”或“基本安全无效”仿制药也成为公众用药安全的隐忧,也造成了医疗资源极大浪费。
随着新版GMP对国内制药行业的调整,药企的生产水平将有整体提高。随着仿制药质量和疗效一致性评价的不断推进,将促使制药行业整体洗牌,全面净化药品市场,新药要新、仿药要同,使国产仿制药的竞争力越来越强。
2、坚持需求导向,鼓励自主研发
有157种过期进口药品,国内没有仿制品上市,进口的原研药价格降价,首先得把这些产品尽快在市场上以国产仿制药进行研发替代。培育具有核心竞争力的企业,而核心竞争力来自有自主知识产权的产品和技术。
3、完善审评审批,提高药品质量
审评审批是仿制药进入市场的源头,是后续管理工作的基础和重要依据。药监局责任重大,燃烧小宇宙吧。
4、政府要加强引导和支持
我国药物研发生态链尚处于起步阶段,很多环节脱节,在研发、产业化等环节方面亟待完善。政府应加强引导,既要提供资金帮助,也要在政策上给予支持,如增加临床试验基地的数量、增加新药审评绿色通道、保护市场独占权、顺利对接医保,提高市场回报率,激励企业加强投如。
5、重视国际化进程
参考印度等发展中国家支持本国企业发展的经验,结合“一带一路”政策,带领国内的仿制药企业尽快走出国门。企业应调整产业结构,培养能够参与国际市场竞争的人才,积极参与国际合作。就像大海一样,把自己放在低处,才能海纳百川,蓬勃发展。
6、加强宣传营销
如今已经不是酒香不怕巷子深的社会,优质仿制药还需走出来让医患人员知道。仿制药宣传还需国家和企业共同努力。
更多资料请参考中商产业研究院发布的《2018-2023年中国仿制药市场前景调查及投资机会研究报告》。
 如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。
如发现本站文章存在版权问题,烦请联系editor@askci.com我们将及时沟通与处理。

